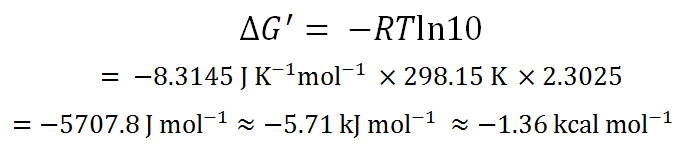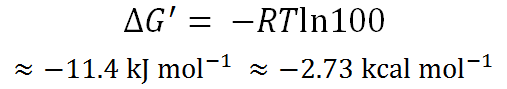薬物による薬理活性は、ターゲットと薬物が、可逆的に結合することによって生じる。
薬物をD, ターゲットをT, 複合体をDTとすると、
以下のような平衡関係を考えることができる。
平衡定数をKとすると、平衡定数と薬物濃度の関係は、以下のように記述される。
また、ギブズエネルギーGと平衡定数の関係は、以下のように記述される。
ただし、Hはエンタルピー, Sはエントロピー, Rはモル気体定数, Tは熱力学的温度である。
ここで、ある2つの状態、【状態1】と【状態2】を考える。
平衡定数の比を考えると、以下のように記述されることが分かる。
上式は、「薬理活性とギブズエネルギーの関係」を考える際に有益である。
□ 活性とギブズエネルギーの関係
薬理活性を10倍にするためのギブズエネルギーの値を求めたいとする。
これは要するに、K2/K1 = 10 ということである。
標準状態を仮定し、上式に値を代入して計算をしてみると、
となる。
つまり、薬理活性を10倍にあげようとすると、
-5.7 kJ/mol (-1.4 kcal/mol) のギブズエネルギーの安定化が必要になる。
同様のロジックに基づき、100倍, 1000倍, 10000倍の場合を考えてみる。
結果は、以下の通りである。
■ 100倍の活性向上
■ 1000倍の活性向上
■ 10000倍の活性向上
上記の値は、暗記しておくと便利である。
ただしこれらは、標準状態における計算値である。
ターゲット付近の温度状況によっては、エントロピー項の寄与が、若干の修正を受ける。
以上の話をグラフ化すると、以下のようになる。
横軸は平衡定数の比、縦軸はギブズエネルギーである。
Figure 1. 0 ~ 1000倍
Figure 2. 0 ~ 10000倍
HTSなどを通じて取得されるヒット化合物の活性は、
通常、数μM ~数十μM 程度であることが多い。
一方、開発候補化合物(CAN)に求められる薬理活性は、
通常、数nM 程度である。
したがって、我々は構造活性相関研究(SAR)を通じて、
薬理活性を1000倍~10000倍程度、改善しなければならないわけである。
これをギブズエネルギーに換算すると、
必要な安定化エネルギーは、
-17 kJ/mol ~ -23 kJ/mol
(-4.1 kcal/mol ~ -5.5 kcal/mol)
となる。
リード化合物の構造最適化を通じて、
これだけのエネルギー安定化の要因を、新たに創出しなければならない。
さて、開発候補品に求められる薬理活性は、通常、数nM 程度であると述べた。
これはすなわち、平衡定数の逆数である 解離定数 Kd に、
同程度の水準が求められるということである。
したがって、必要な平衡定数は、10の9乗程度のオーダーであることが分かる。
ここから、ギブズエネルギーを計算すると、
となる。
開発候補品に求められるギブズエネルギーの安定化は、
-51.4 kJ/mol (-12.3 kcal/mol) 程度であることが分かる。
↓応援クリックしてくれると励みになります!